|

↑Source: Waheed A, et al. Oncology (Williston Park).
2024;38(12):472-474.
◎文╱藥師施如亮
一、簡介:
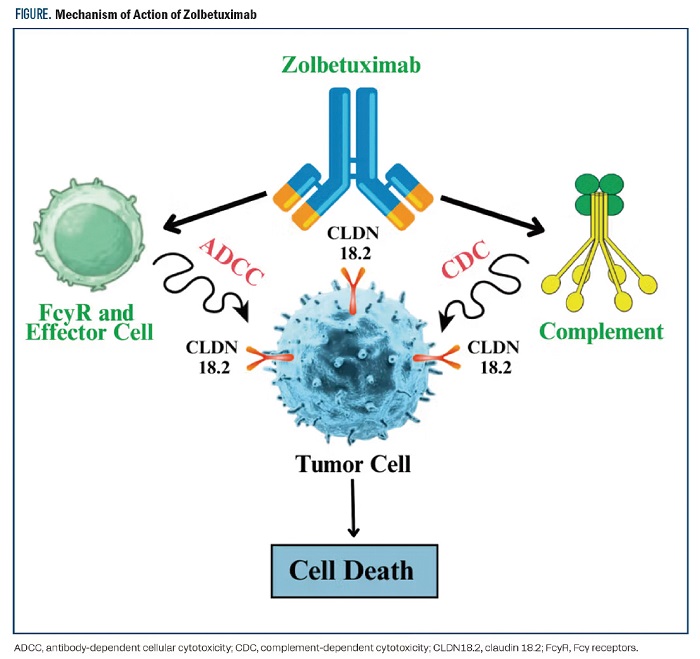
CLDN18.2是一種高度特異性的跨膜蛋白,主要存在於正常胃黏膜中。在胃癌、胰臟癌等多種惡性腫瘤中,CLDN18.2會異常高表達並暴露,使其成為精準免疫治療(如
ADC、CAR-T)的熱門「標靶」。Zolbetuximab為重組嵌合單株抗體,能特異性結合於胃癌細胞表面的CLDN18.2。一旦結合完成,它會利用抗體的Fc區域引發體內的免疫反應。透過啟動抗體依賴性細胞毒性作用(ADCC)與補體依賴性細胞毒性作用(CDC),有效達成破壞癌細胞的效果(機轉如圖)。
二、健保共同擬訂會議決議:
本案為針對 CLDN18.2 的單株抗體藥物。依據SPOTLIGHT臨床試驗結果顯示,zolbetuximab 併用mFOLFOX6
相較於安慰劑併用mFOLFOX6,在無惡化存活期中位數 (10.6個月 vs. 8.6個月) 及整體存活期中位數 (18.2個月 vs.
15.5個月) 均呈現較佳結果。考量其臨床效益,且廠商同意與健保署簽訂藥品給付協議,爰同意納入健保支付項目,屬第2A類新藥。
三、給付規定:
9.133 Zolbetuximab (如Vyloy®):(115/4/1)
1.限與含氟嘧啶(fluoropyrimidine)和含鉑的化療藥併用,適用於CLDN18.2陽性、第二型人類表皮生長因子受體(HER2)陰性的局部晚期不可切除或轉移性胃腺癌病人的第一線治療,且符合下列條件:
⑴病人身體狀況良好(ECOG≦1)。
⑵初次申請時需檢附確實患有局部晚期不可切除或轉移性胃腺癌之病理或細胞檢查報告,及以免疫組織化學染色法確定腫瘤為CLDN18.2陽性(定義為≥75%的腫瘤細胞顯示中至強染色強度的CLDN18.2)且第二型人類表皮生長因子受體(HER2)陰性之檢測報告。
2.須經事前審查核准後使用,每次申請事前審查之療程以12週為限,再次申請必須提出客觀影像學證據(如:RECIST
criteria)證實無惡化,才可繼續使用。
3.本案藥品與免疫檢查點抑制劑僅能擇一給付,且治療失敗時不可互換。
資料來源:
1150225_全民健康保險藥物共同擬訂會議藥品部分第80次會議紀錄第5頁_討論提案第4案

(本文作者為前中央健康保險署醫審及藥材組組長)
回首頁 |